Чи достатньо миття рук для захисту від коронавіруса?
Ми і раніше зустрічали людей, які дуже завзято і впевнено говорили «Що? Коронавірус? Просто мийте руки з милом і все буде добре!». А зараз такі люди чомусь почали об’єднуватися і захоплювати уми населення. І вже в пошуковій видачі Google можна зустріти «Мило як нова релігія» або «В боротьбі з коронавірусом ефективно будь-яке мило!».
Важко сказати, чи є якийсь прихований в цьому всьому сенс (як прихований сенс в інстаграм-рухах антимасочників і т.п.) і чи є сенс цей сенс шукати. У даному огляді ми розглянемо, чому, з точки зору колоїдної хімії, мило від коронавіруса не допоможе (так само як і спирт) і чому найкраще користуватися перекисом водню, а десь і навіть гіпохлоритом. Розглянемо механізми дії миючих засобів в епоху пандемії коронавируса та проведемо критичний аналіз наявної інформації, оскільки дурістю і самовпевненістю Ні віруси, ні бактерії точно не перемогти...
1. Мило та дезінфекція
І інструкція ВООЗ і безліч інших документів свідчать - милом ми змиваємо забруднення, а антисептиком дезінфікуємо руки. Начебто все гранично ясно. Мило - миє, дезінфектант - дезінфікує. Але періодично в деякі гарячі голови, частіше всього від нестачі освіти і бажання вірити чомусь іншому крім газет і пабліків в соцмережах, приходить помилкова думка - «А навіщо шукати антисептик, помию я просто руки милом і все».
Почнемо з того, що є речовини, які впливають на мікроорганізми, а є речовини які на них не впливають. Ті, які мікроорганізми знищують або зупиняють їх зростання - називаються протимікробними агентами. Всі протимікробні агенти можуть класифікуватися відповідно до їх функцій. Мікробіоцідні - знищують мікроорганізми, біостатичні - уповільнюють і пригнічують їх зростання.
Основними класами мікробіоцідних агентів є:
Дезінфектанти - неселективні «грубі» хімічні сполуки, які інактивують або знищують широкий спектр мікроорганізмів на інертних, неживих поверхнях. Дезінфікуючі засоби діють, руйнуючи клітинну стінку бактерій або порушуючи їх метаболізм. Дезінфекцію не варто плутати зі стерилізацією, яка знищує всі без винятку види мікроорганізмів, тому що наприклад бактеріальні спори не всякий дезінфектант в силах пошкодити. До цієї групи належать спирти, альдегіди, пероксикислоти, феноли, четвертинні амонієві сполуки, неорганічні кислоти, галогени і т.п.
Антисептики - такі ж, не особливо селективні сполуки, але які наносяться на живі тканини або шкіру для того, щоб знизити ризик зараження (запобігти розвитку хвороби). Деякі антисептики мають істину бактеріоцидну дію, тобто знищують мікроби в прямому сенсі, а деякі є бактеріостатичними, тобто запобігають або сповільнюють ріст бактерій. Антисептики, які здатні дезактивувати або руйнувати віруси, називаються віруліцидами (або віруцидами, як кому зручніше). Сюди відносяться всі ті ж спирти, хлоргексидин (згадаємо і октенідин), розчин Дакіна, медичний перекис водню, спиртова настойка йоду, гіпохлорит натрію (в ветеринарії) і т.п.
Антибіотики - досить селективні сполуки, що працюють з вузьким спектром мікроорганізмів, і знищують їх усередині організму-носія (людського тіла або тіла тварини). Серед прикладів можна назвати тетрациклін, азитроміцин, пеніцилін та інші. Речовини східного функціоналу, але селективні до вірусів - називаються противірусними препаратами. Головна їхня відмінність від антибіотиків в тому, що противірусні препарати не знищують вірус, вони просто перешкоджають його розвитку. Так само справа йде і з протигрибковими препаратами, протипаразитарними і навіть зі сперміцидами.
Біоциди - функціональний аналог дезінфектантів, але призначений для знищення всіх форм життя, а не тільки мікроорганізмів. Це можуть бути як хімічні речовини, так і мікроорганізми. У цю групу входять пестициди, інсектициди, родентициди всякі і навіть репеленти + атрактанти.
Для всіх груп речовин ключовим словосполученням є «наявність доведеної здатності впливати на мікроорганізми».

Як ми бачимо, мило не потрапляє в жодний з наведених класів речовин. В якості аналогії можна сказати, що якщо в якихось особливих умовах відвар моркви знищив золотистого стафілокока - це не привід використовувати його для обробки лікарень. Хоча також можна сказати, що ситуація з COVID-19 розвивалася надто стрімко, щоб вивчити вплив мила. І при цьому не важливо, що коронавіруси відомі досить давно, як і безліч інших вірусів з ліпідними мембранами, для видалення яких ніхто не радить застосовувати мило. Можна також згадати вірус сказу, вірус гепатиту, вірус Зіка, лихоманку Денге, а також дуже небезпечний вірус Марбург (цікаво, що відповіли мікробіологи, які його вивчали на пораду «просто мийте руки з милом!»).
Отже, зробимо висновок №1 - для ПАР не прийнято говорити про мікробіоцідний вплив на мікроорганізми. Є дані щодо зниження обсіменіння, що цілком укладається в концепцію миття рук. Миємо для того, щоб прибрати забруднення. Можемо навіть оцінити ступінь очищення. Але не дезінфікуємо.
2. Особливості будови коронавіруса
Розглянемо, як влаштовані коронавіруси (в т.ч. і SARS-CoV-2, який є причиною COVID-19). В цілому це, фактично, «кулька жиру» з якого виходять білкові відростки різної, довжини.
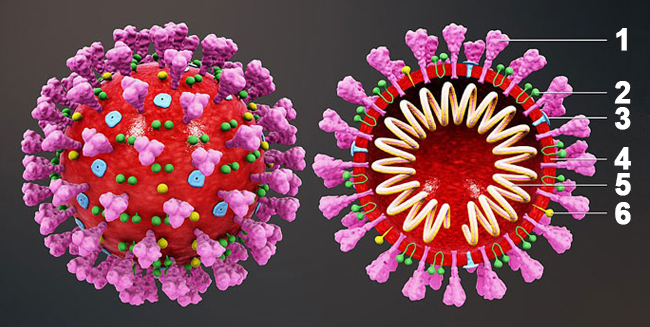
1 - структурний білок (глікопротеїн) шипа (S),
2 - структурний білок (глікопротеїн) мембрани (E),
3 - поверхневий білок гемаглютинестераза (HE),
4 - оболонка,
5 - РНК і білковий нуклеокапсид («кишенька для РНК ») (N),
6 - структурний білок (глікопротеїн) оболонки (M).
Співвідношення білків гликопротеинов №6, №1 і №2 - 1:20:300. В середньому частка коронавируса має 74 шипа №1. Кожен шип довжиною близько 20 нм. Сама кулька розміром 85-100 нм (0,08-0,1 мкм).
Коронавірус - це вірус оболончатий (англ. Enveloped). З чого ж ця оболонка складається? Оболонка складається з фосфоліпідів та білків, що знаходяться в проміжках між ними (№1, №2, №3, №6). Фосфоліпіди виглядають приблизно так:
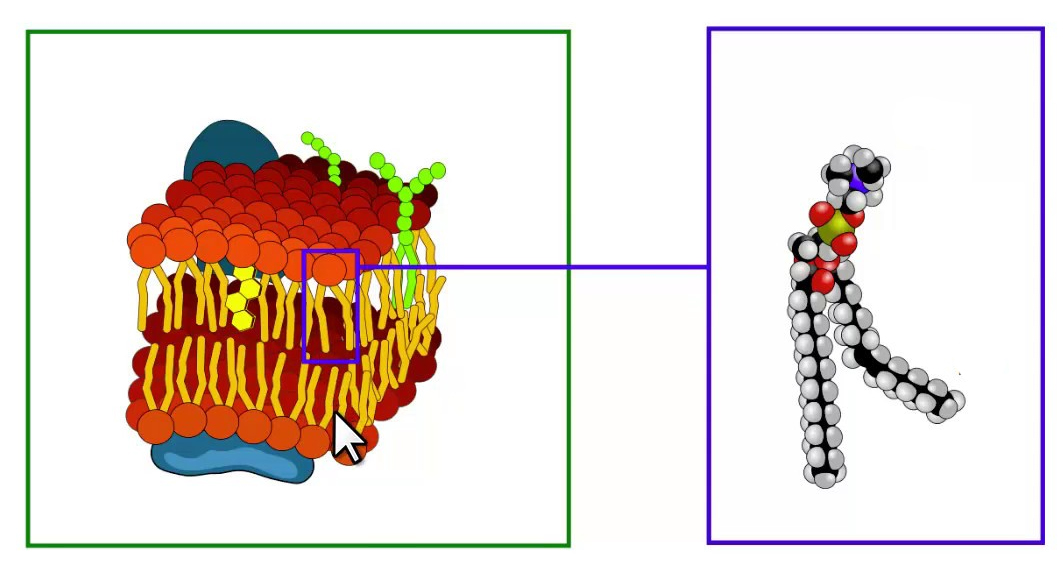
Фосфоліпіди - це речовини, які складаються з полярної гідрофільної «голови» і гідрофобного «хвоста». У разі фосфоліпідів «голова» - це негативно заряджена фосфатна група, а «хвіст» - ланцюги жирних кислот, поєднано все це між собою через молекулу гліцерину.
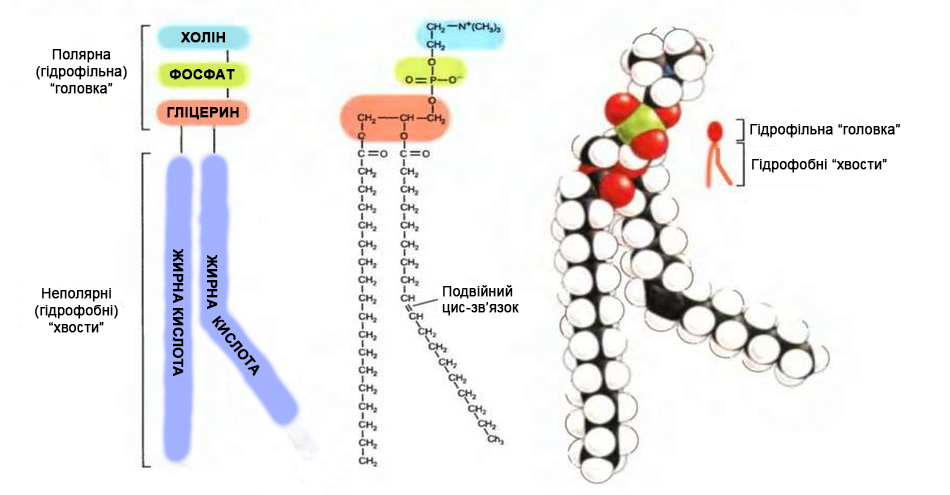
Гідрофобність «хвостів» полягає в тому, що вони виштовхуються з води (а гідрофільність «голів» - в тому, що вони в воду занурюються). Одночасне бажання кожного хвоста вилізти з води призводить до того, що вони формують певну гребінку-моношар, для мінімізації взаємодії з молекулами води. Часто доводиться чути слово амфіфільні (раніше більше застосовували «дифільні») в застосуванні до фосфоліпідів. Воно означає що речовина може одночасно проявляти як гідрофобні, так і гідрофільні властивості, в залежності від орієнтації своєї молекули. Такими властивостями володіють поверхнево-активні речовини (ПАР), багато білків (і пептиди), полімери.
Завдяки такій, нестабільної в рідких середовищах, структурі подібні молекули можуть агрегувати з утворенням різних надмолекулярних структур (мицелл, бішарів - подвійних шарів, ліпосом і т.п.). Наприклад ліпідний бішар виникає, коли гідрофобні хвости шикуються в лінію один проти одного, утворюючи мембрану з гідрофільних головок з обох сторін, звернених до води. Форма агрегатів (надмолекулярних структур) залежить від хімічної структури поверхнево-активної речовини, а саме від балансу в розмірах між гідрофільною головкою і гідрофобним хвостом. Міра цього - гідрофільно-ліпофільний баланс (ГЛБ). Не дивлячись на багато переваг, шкала ГЛБ не враховує додаткові властивості, пов’язані з поділом зарядів і гідрофільних груп, і не передбачає поведінку речовин в відношенні, наприклад, білків. Працюють також і інші механізми.
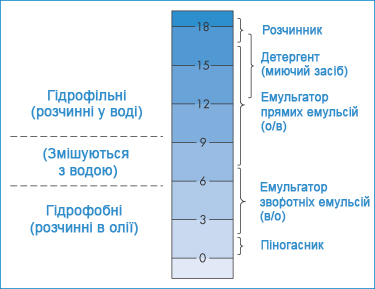
Всі мембрани, моно- і бішари, ліпосоми і т.п. - все це утворюється і утримується поруч один з одним завдяки зв’язкам слабким і хемілюмінесцентним, нековалентним силам міжмолекулярної взаємодії (в тому числі силам Ван-Дер-Ваальса - дисперсійним силам Лондона/Дебая/Кеезома). Їх масштаби можна оцінити за допомогою картинки (і зіставити з «найпотужнішими» зв’язками, на зразок іонних - як в неорганічних солях, металевих - як в металах, або ковалентних - як в який-небудь органіці):
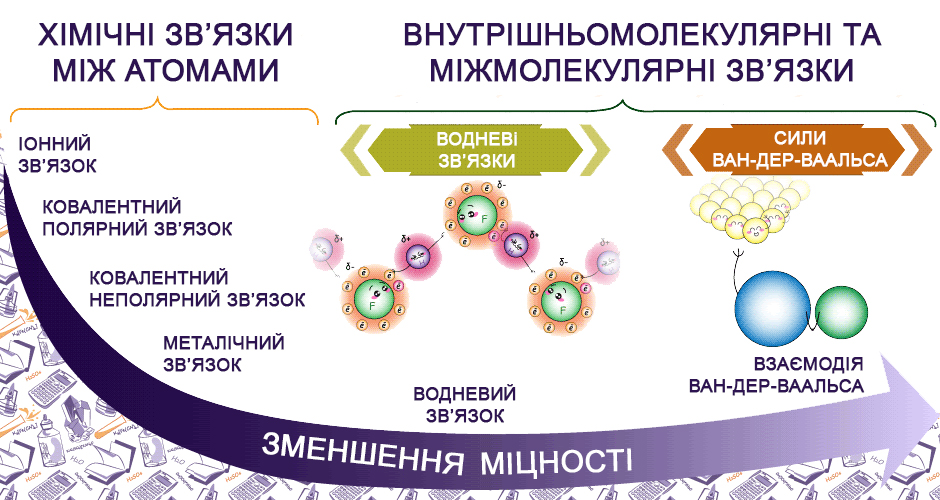
Нижче показано, де ці взаємодії (зокрема слабкі) можна побачити в реальному житті. Найкраще це ілюструється на прикладі механізму змішування різних рідин (так, рідини розчиняються одна в одній завдяки наявності слабких взаємодій):
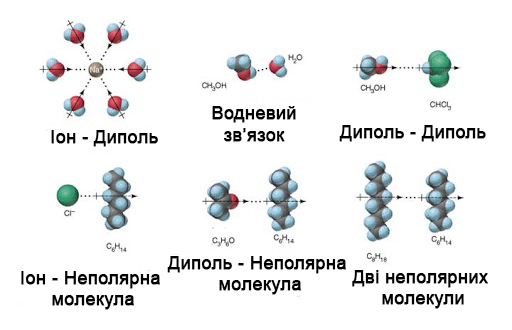
Тепер потрібно підсумувати, що сіль розчиняється у воді завдяки іон-дипольній взаємодії, а метанол (а також етанол та інші спирти) змішується з водою завдяки утворенню водневих зв’язків.
Ліпідна оболонка вірусу, надмолекулярні структури з РНК і білків - все це зібрано і утримується разом тільки за рахунок слабких взаємодій, ніяких ковалентних (а тим більше, іонних і металевих зв’язків) там зовсім немає. Тобто молекули (ті ж ліпіди в мембрані) "прилипають" одна до одної. Між іншим, до поверхонь і шкірі вірус так само кріпиться, переважно, за рахунок водневих зв’язків. Також можуть бути гідрофільні або ліпофільні взаємодії - по суті «розчинення», яке виникає теж завдяки утворенню слабких зв’язків.
Система, яка побудована на слабких взаємодіях - досить динамічна і гнучка. Весь оточуючий нас світ, вся колоїдна хімія на відміну від традиційних речей на зразок хімії неорганічної, або біохімії, будується на прив’язці НЕ до взаємодії сильних зв’язків, а до комбінацій зв’язків слабких.
Безліч найбільш важливих хімічних і фізичних процесів на нашій планеті відбуваються на поверхні або межі розділу між фазами (тверда речовина - рідина, рідина - газ і т.п.). Межа розділу (англ. Interface) - це перехідний шар між двома фазами або поверхня дотику між об’єктами. Атоми і молекули на межі розділу проявляють абсолютно інші властивості, ніж атоми і молекули в об’ємі фази або матеріалу.
3. Механізм дії мила
Наскільки ж тісний зв’язок мила та коронавіруса?
Спробуємо це з’ясувати, поки «коронавірус крокує по планеті». Об’єкти ці співіснують тисячі років. Епідемії крокують, а мило - миє. Притому миє тисячоліттями.
А чому воно миє? Досить давно відомо, що поверхнево-активні речовини проникають-прилипають-адсорбуються до грудочок бруду, дроблять їх, а потім з роздробленими «запчастинами» спливають на поверхню води.
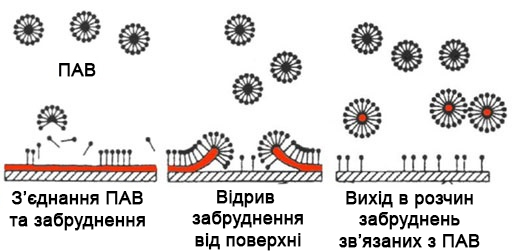
Перший запис про мило, як таке, був знайдений в стародавньому Вавилоні, датується 2200 до н.е. і описує приготування мила з води, лугу (з кісткового попелу) і масла касії (звична нам кориця). Варто згадати, що і древні єгиптяни, які захоплюються купанням, виготовляли мила з рослинних і тваринних жирів в поєднанні з лужними солями. Відомий давньоримський медик Гален у своїх роботах прямим текстом згадував про використання лугу (гідроксиду натрію) для виготовлення мила.
Перша згадка про застосування миття рук для медичної гігієни можна віднести до робіт Ігнаца Філіпа Земельвейса - угорського лікар-акушера 19 століття, одного з основоположників асептики, «батька методики обробки рук». В архиві Беттманна збереглася фотографія, на якій Ігнац Земмельвейс миє руки в хлорній вапняній воді перед операцією.

Ну і як то вже так повелося, що найпростіший і найдоступніший спосіб забезпечення чистоти рук - це їх миття. Ну а мити доводиться як - водою з милом і не «по Земмельвейсу», він використовував гіпохлорит. У деяких випадках, до речі, вода з потрібною гідродинамікою, яка може бути важливіше ПАР, може дати непоганий результат. Внесення мила в рівняння у процес дозволяє підвищити ефективність, але не до рівня Земельвейса. Зупинимося на цьому простому, але не дуже, об’єкті докладніше.
Розповідь почати варто з самого визначення. Російська Вікіпедія нам говорить:
«Мило - рідкий або твердий продукт, поверхнево-активна речовина, в поєднанні з водою використовується для очищення і догляду за шкірою».
Українська Вікіпедія дає дещо інше, більш енциклопедичне визначення:
«Мило — розчинна у воді мийна речовина, як хімічний продукт являє собою відносно складне з’єднання жирних кислот з лугами, а за своєю будовою відноситься до класу солей. Випускається в твердому стані, рідкому, а також у вигляді порошку і гранул».
Вікіпедія англійська, також, традиційно, більш енциклопедична, і стверджує, що:
«Мило - це сіль жирної кислоти, яка в домашніх умовах використовується для прання і т.п.»
Зате на відміну від російської та української Вікіпедії, в англомовному варіанті присутня ось така цікава інформація (обведено):
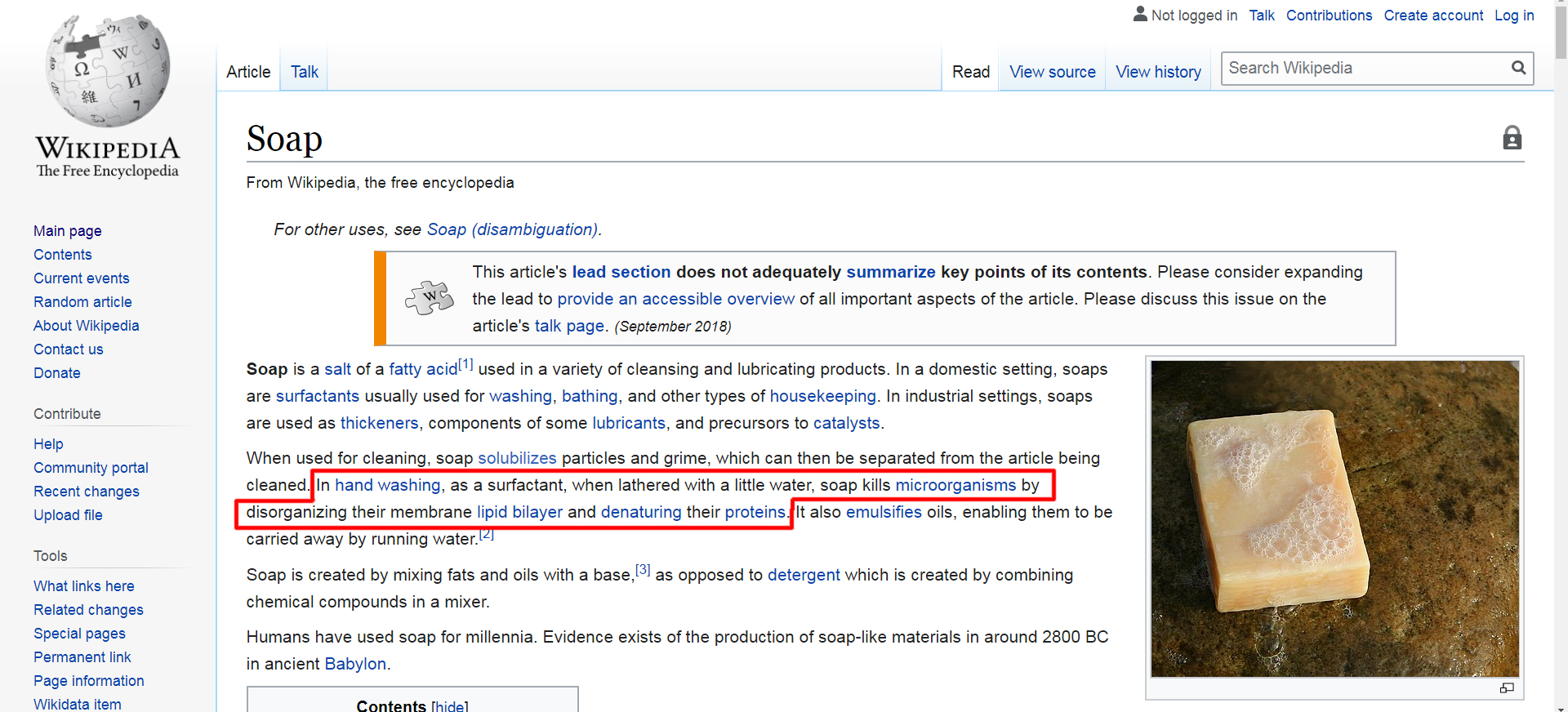
Тепер ми бачимо, звідки взялася інформація про те, мило замінить всі антисептики.
У вільному перекладі там написано приблизно наступне «Під час миття рук, як поверхнево-активна речовина, мило вбиває мікроорганізми, дезорганізуючи їх мембранний ліпідний двошаровий шар і денатуруючи їх білки».
Після вказаної тези наведено посилання на статтю Чарльза Тумоса 2001 року під назвою «Коротка історія алюмінієвого стеарату як складової фарби», в якій описано використання мила в якості допоміжного компонента в складі олійних фарб, але жодним чином не згадуються мікроорганізми, мембранний ліпідний двошаровий шар та денатурація білків.
І хоча під час пандемії та для ресурсу рівня Вікіпедії посилання на подібні твердження як мінімум повинні були вірними, але залишимо це на совісті тих, хто це написав.
Ну а тепер зупинимося докладніше на цьому моменті. Отже загальновідома зараз думка говорить, що поверхнево-активні речовини розчиняють ліпідну двошарову мембрану віріонів, хоча при детальному розгляді виявляється, що точний механізм цієї дії невідомий, так само як немає і стрункої картини відмінності ефектів різних ПАР на різні віруси в різних умовах. Та що там казати, про віруси, ПАР працюють навіть з мембранами в лабораторній пробірці далеко НЕ по одному механізму. Фактично, скільки є ПАР, стільки є і механізмів. Логічно, що в залежності від просторової структури молекули можуть відбуватися різні механізми вбудовування в ліпідну мембрану, а не так як демонструють в деяких популярних відео - захопили дві молекули «мила» шматок вірусу і понесли геть... Тому потрібно відмітити, що насправді життя дещо складніше ніж будь-яке, навіть саме барвисте відео на Youtube.
Ще з кінця минулого століття, застосовуване до клітинних мембран, найчастіше вважалося що ПАР позбавляють мембрану бар’єрних властивостей за рахунок збільшення проникності. Притому, практично скрізь обмовлялося, що цитотоксичні клітинні ефекти залежать як від абсолютних концентрацій, так і від молярних відносин ліпід - ПАР. Найчастіше еквівалентні або просто високі концентрації ПАР викликають лізис клітин. Тобто обґрунтована відповідь на питання «як ПАР діє на клітини?» - це порушення цілісності клітинної мембрани і лізис клітин (по суті і то і то можна вважати «мембранними процесами»).
Лізис (грец. Λύσις «поділ») - це розчинення клітин і їх систем, в тому числі мікроорганізмів, під впливом різних агентів, наприклад ферментів, бактеріолізинів, бактеріофагів, антибіотиків. По суті це руйнування мембрани клітини. У лабораторіях молекулярної біології, біохімії і клітинної біології клітинні культури можуть піддаватися лізису в процесі очищення їх компонентів, таких як очищення білка, екстракція ДНК, екстракція РНК або очищення органел. Пеніцилін і родинні β-лактамні антибіотики викликають загибель бактерій в результаті ферментативного лізису, який відбувається після того, як ліки змушують бактерію утворювати дефектну клітинну стінку.
Так як всі функціональні можливості ПАР - залежать від хімічної природи цих речовин, їх концентрацій і умов зовнішнього середовища, то поки варто зупинитися саме на цьому. Принаймні на тих загальних моментах, які в подальшому спростять розуміння мембранних проникностей - солюбілізацій - міцелоутворення і т.д.
В якості ПАР можна вважати будь-яку речовину, яка впливає на поверхневий натяг. Для тих, кого таке формулювання не влаштує - запропоную інше: «речовина, яка адсорбується на кордоні розділу фаз». ПАР в плані «мило» (тобто «колоїдними» або «міцелярними») можна вважати тільки ті речовини, які здатні утворювати міцели. Низькомолекулярні спирти, аміни і кислоти з невеликою довжиною вуглеводневого залишку (менш десяти груп -CH2-) як ПАР можуть вважатися, та ось миючими властивостями не володіють. Тому далі будемо говорити більше про ПАР, які здатні мити.
Існує багато різних різновидів таких ПАР, класифікованих по тому, який заряд несе на собі їх гідрофільна «голова» (і чи несе вона його взагалі):
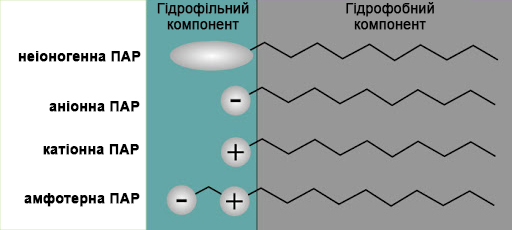
Аніонні несуть негативний заряд, катіонні - позитивний заряд, амфотерні - позитивний або негативний залежно від рН середовища різному - в кислому розчині проявляють властивості катіонних ПАР, а в лужному розчині - аніонних ПАР, а неіоногенні - нейтральні. Все іоногенні ПАР після іонізації в розчині утворюють поверхнево-активні іони, неіоногенні ПАР не дисоціюють, поверхневою активністю володіє вся молекула.
Не варто думати, що ПАР і мила - вони є тільки десь там, в далеких миловарнях і на жирових комбінатах. Є й цілком собі біогенні, присутні в кожній людині з дитинства.
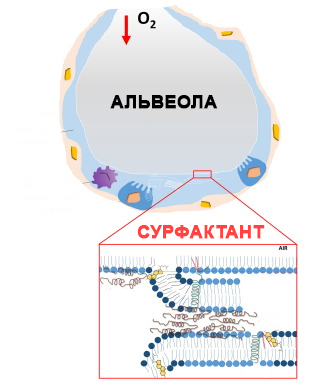
Першим важливим прикладом може служити легеневий сурфактант - ліпопротеїновий комплекс, завдяки якому ми можемо дихати. По суті - це комбінація поверхнево-активних речовин, що вистилає легеневі альвеоли зсередини. Основний склад - це 40% діпальмітоілфосфатіділхолін, 40% інших фосфоліпідів, 10% поверхнево-активних білків (вони ще називаються колектіни), 10% холестерину. Основна функція цієї суміші ПАР полягає в зменшенні поверхневого натягу на межі поділу повітря/рідина в легенях. Секретується клітинами пневмоцитами з компонентів плазми крові. Між іншим, саме на поверхні пневмоцитів знаходиться велика частина АПФ-2 він же ангіотензинперетворюючий фермент 2 - точка входу коронавіруса в організм:
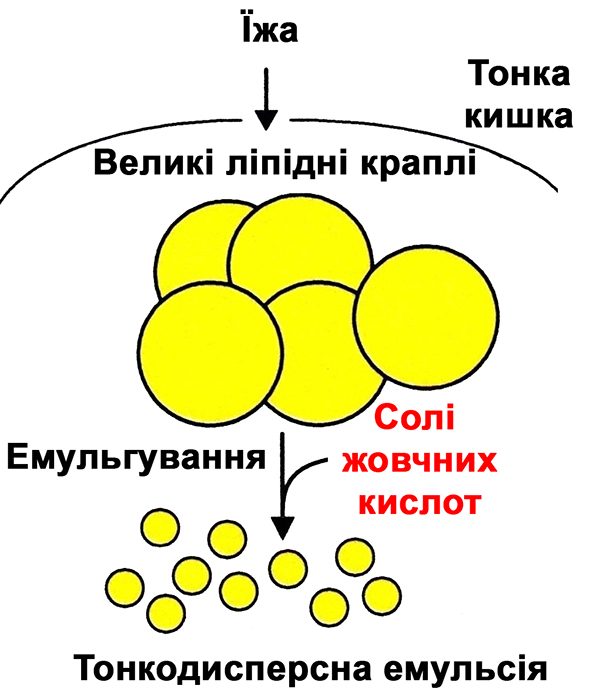
Другий важливий приклад - це жовчні кислоти. Нагадаємо, що жовч - це лужний секрет, що виробляється гепатоцитами печінки. Він накопичується в жовчному міхурі і виділяється в дванадцятипалу кишку, як тільки в ній з’являється їжа. Основна функція жовчі - допомогти переварити (емульгувати) жири. Жовчні кислоти - це не зовсім традиційні ПАР з точки зору структури і поведінки. Синтезуються вони з холестерину і мають стероїдну структуру. Жовчні кислоти орієнтується паралельно уздовж кордону розділу фаз, на відміну від традиційних поверхнево-активних речовин які орієнтуються перпендикулярно. Тому красиві щільно упаковані надмолекулярні структури за допомогою жовчних кислот та їх солей не одержати, у них мета одна - обволікати і поглинати.
Розглядаючи механізм ушкодження мембран за допомогою ПАР також потрібно згадати таку річ як ККМ (Критична Концентрація Міцелоутворення) - це така концентрація ПАР, при якій індивідуальні молекули ПАР починають самоорганізовуватися у міцели.
Міцела - це об’єднання з молекул ПАР, що знаходяться у водному середовищі. Міцели можуть бути невеликими сферами або дисками (як згадані вище жовчні кислоти), сплющеними або витягнутими еліпсоїдами, довгими циліндрами, двошаровими та пласкими (бішари) або навіть формувати якісь кубічні фази. Побачити все це можна тільки за допомогою одного методу - Кріоелектронної мікроскопії.
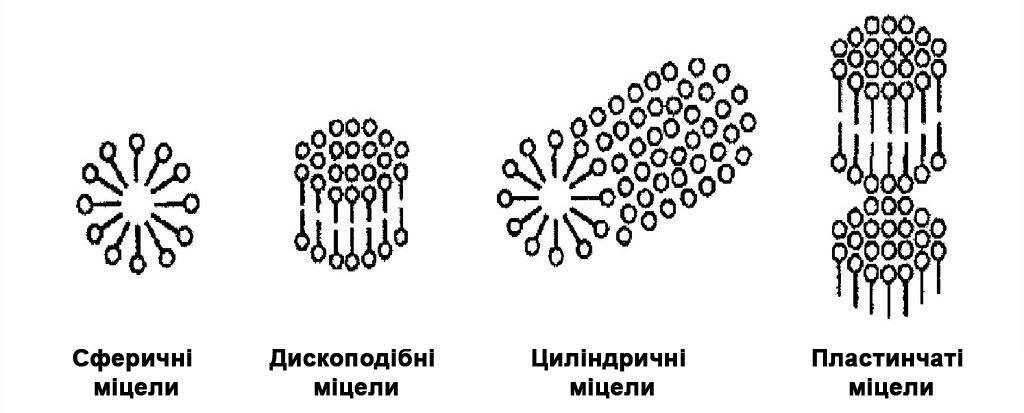
Форма одних і тих же ПАР часто залежить від їх концентрацій у воді. По досягненню ККМ найчастіше утворюються маленькі сферичні міцели. Далі зі зростанням концентрації ПАР «кульки» (в лапках, тому що насправді сферичні міцели не зберігають симетричну форму і не мають ідеально прилягають одна до одної гідрофільними «головами», просто так їх звичайно зображають) перетворюються на червоподібні/дископодібні міцели або в «міцели всередині нашого організму» - везікули:
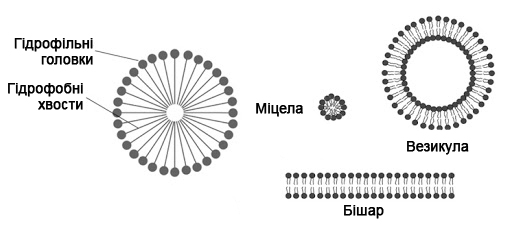
Перехід від одного типу міцели до іншого може протікати як мимовільно, так і керовано (за допомогою, знову ж таки, підвищення концентрації ПАР до рівня «другої ККМ»). Термічний вплив на «голову» теж призводить до зростання міцел. Для деяких ПАР (зокрема неіоногенних) температуру, при якій гідрофільна група максимально зневоднена і ПАР відділені від водної фази, ще називають точкою помутніння і використовують для ідентифікації конкретних речовин.
До речі, міцели іоногенних ПАР при високих температурах розпадаються на більш дрібні асоціати - димери і тримери (деміцелізація). Тому в окропі мило мити не буде (так само як і в крижаній воді). А в теплій - працює, тому що досягається оптимальна концентрація ПАР.
При низьких концентраціях поверхнево-активні речовини утворюють істинні розчини. Істинний розчин, це наприклад, розчин чаю/цукру в склянці, тобто ніяких там структур не утворюється. З ростом концентрації і наближенням до ККМ починають формуватися надмолекулярні структури з міцел і істинний розчин переходить в колоїдний (або міцелярний). Вище ККМ весь надлишок ПАР знаходиться в вигляді міцел. При дуже великому вмісті ПАР в системі взагалі утворюються рідкі кристали (ліотропні мезофази) або гелі.
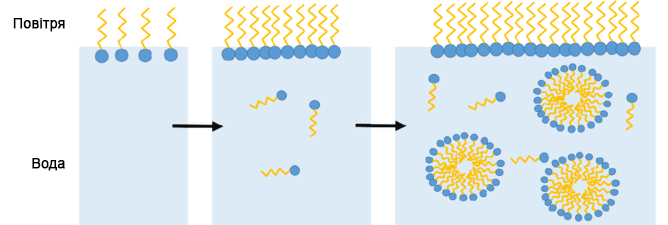
При розведенні розчину міцели розпадаються, а при збільшенні концентрації ПАР знову виникають, тобто процес зворотній. Розуміння, що таке ККМ в застосуванні до ПАР настільки ж важливо, як і розуміння, що таке температура в застосуванні до лазні, наприклад. Але на відміну від температури, яку вимірює будь-який копійчаний термометр, значення ККМ для якихось певних поверхнево-активних речовин знайти і визначити не так-то й просто.
В цілому, ККМ може ще й виступати в ролі такого собі суб’єктивного критерію для оцінки ефективності ПАР («що краще буде мити»). Хоча в разі поверхнево-активних речовин складно сказати яке краще, яке гірше. Найчастіше тут оперують декількома комплексними критеріями порівняння, на кшталт:
- Чим нижче ККМ, тим краще ПАР може самоорганізовуватися з утворенням міцел, а значить тим менше речовини знадобиться для взаємодії з гідрофобними сполуками.
- Чим краще знижується поверхневий натяг на межі повітря-вода - тим краще поверхнево-активні речовини можуть упаковуватися на кордоні розділу повітря-вода (орієнтуючи вуглеводневі ланцюги в напрямку повітря і гідрофільні групи в напрямку водної фази).
- Наскільки хороший ефект емульгування, тобто наскільки добре ПАР стабілізують суміші води (гідрофільне) і олії (гідрофобна), що не змішуються в звичайних умовах, у вигляді мікроскопічних крапель однієї рідини в іншій. Чим вище ця здатність, тим легше буде відмиватися жир.
Однією з великих «білих плям» сучасної колоїдної хімії можна вважати відсутність систематичних досліджень, які б зачіпали широкий спектр ПАР в застосуванні до вивчення якоїсь характеристики, інакше складно екстраполювати. Як правило, прийнято мати справу з чимось одним. Пов’язано це з тим, що ККМ, а значить і пов’язані з цим параметром механізми міцелоутворення і ефективності ПАР, дуже чутливі і до температури, і до іонної силі розчину, і до рН. Тому якщо в лабораторному світі дослідження ще якось можна привести до спільного знаменника, то в разі масштабування на реальний світ (наприклад, «чим руки мити від коронавіруса») побудувати якісь об’єктивні прогнози поведінки ПАР практично нереально - надто багатофакторна потрібна оцінка. Тому бездумно підбирати інформацію з наукових статей і проектувати її на широкий побут, це як мінімум нерозумно, а як максимум, дарує представнику того самого широкого побуту почуття удаваної безпеки.
Розчини, що містять тільки ПАР або тільки один вид ПАР, слабо виявляють деякі колоїдно-хімічні властивості, наприклад, характеризуються слабкою пептизуючою здатністю (здатністю до дроблення забруднень), надають недостатню стабілізуючу дію і не запобігають вторинному осіданню частинок і т.д. Згадати можна відомий багатьом приклад серйозного недоліку звичайних жирових мил, коли іони магнію, кальцію та інших багатовалентних металів утворюють з аніоном мила нерозчинні солі, що не володіють поверхневою активністю. Тому звичайне мило погано миє в «жорсткої» воді і зовсім не миє в морській. Розуміючи це, складно навіть думати про те, наскільки ефективно будуть видалятися віріони, тут би розібратися з простими забрудненнями...
Таким чином, висновок №2 - всі напрацювання, пов’язані з «ПАР руйнує ліпідні мембрани» відносяться тільки до лабораторних досліджень. Там, де присутні модельні системи з чистих ПАР, з відомою концентрацією, з конкретними чистими ліпідами, з контрольованою температурою та рН. І при всьому цьому, до сих пір немає єдиної думки про механізми взаємодії і немає порівняння цих механізмів для ПАР різної хімічної природи. Хто з вас, намилюючи руки шматком мила, замислювався над тим, яка концентрація молекул ПАР в утвореному розчині? А рівнятися хочеться на якісь приклади зі статей, де часто ці концентрації відомі з точністю до четвертого знака після коми...
4. Дія мила на ліпідні мембрани
Якщо ж припинити філософські міркування і повернутися до проникності мембран (вивченої в лабораторних умовах), то в цілому, можна сказати, що дійсно поверхнево-активні речовини можуть робити ліпідну мембрану пористою і проникною. Але не завжди, і не всі. Тільки з «висоти» шкільної хімії здається, що всі взаємодії між молекулами прості і немудрі. Насправді в цьому світі багато нюансів.
Так само і у випадку з проникненням ПАР в ліпідну мембрану коронавіруса. Напевно, мало хто зможе представити (без урахування яскравих демонстраційних відео) як насправді молекули поверхнево-активної речовини «поміщають своє тільце» в проміжки між ліпідами мембрани вірусу. Забігаючи вперед скажу, що технічно це схоже на спроби пасажира, що поспішає, втиснутися в переповнений вагон метро.
Крім того, після висловлювання «ПАР роблять мембрану пористішою», потрібно поставити ще одне питання «Роблять за який час?», «Чи не є оборотною ця пора в біологічній, схильній до самосцілення системі?» і т.п. Навіть та ж сама мильна бульбашка - щільно упаковані поруч одна з одної молекули ПАР - лопається, коли утворюється дірка і молекули втрачають контакти з іншими молекулами і не в силах себе самосцілити. Те, як збудовані молекули ПАР, грає одну з найважливіших ролей в процесі зміни колоїдного стану будь-якої надмолекулярної структури. А те, яким буде «лад», пов’язане з параметрами упаковки молекул.
Вперше на це звернув увагу в кінці 70-х років минулого століття колоїдний хімік Джейкоб Н. Ізраелашвілі, який навіть ввів в науковий обіг таку річ, як критичний параметр упаковки ПАР (Р). Параметр цей дозволяв прогнозувати форму і розмір міцел. Стосовно до вірусних мембран, саме від форми залежить і те, наскільки ефективно ПАР зможе формувати нові надмолекулярні агрегати за участю частин від віріона. Навіть на вже згаданому з початку статті відео, ПАР активно впроваджувалися в ліпідну мембрану, та все без толку, віріон лопнув, тільки коли шматки оболонки почали потрапляти в кулясті міцели, а міцели повинні були б сформуватися при концентраціях близьких до ККМ .
Традиційно вважається, що все зав’язано на хімічну структуру і розміри «голови». Велика голова - це сферичні міцели, мала голова - це ламелярні міцели.
На параметр упаковки впливають і багато інших фізичних і хімічних чинників, наприклад, присутність розчинників, що знижують поверхневий натяг. У цьому випадку величина рівноважної площі гідрофільної «голови» збільшується, а значення критичного параметра упаковки (Р) зменшується, тобто бішари переходять в міцели, червоподібні міцели в сферичні і т.д. Робить свій вплив і температура. Наприклад, збільшення температури знижує стеричну перезарядку поліетіленооксидних «голів», зменшується рівноважна площа «голови», P збільшується і сферичні міцели переходять в циліндричні і т.д. Кожен ПАР має свої особливості.
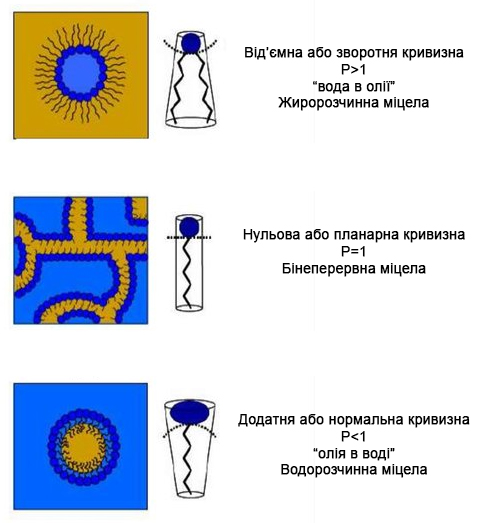
Всі незвичайні властивості об’єктів, що утворилися за допомогою ПАР, зобов’язані тому, що молекули цих речовин можуть вибудовуватися щільними рядами.
Моношари ПАР можуть покривати величезні простори. Наприклад, 0,106 мг стеаринової кислоти («звичайне мило») покриває поверхню води площею 500 см2. При цьому площа поперечного перерізу молекули всього 0,2 нм2, товщина адсорбованої на воді плівки 2,5 нм.
Логічно припустити, що більш щільна упаковка буде там, де або все однакової геометрії, або геометрія взаємнодоповнююча. Геометрія - це певна просторова форма молекули.
В залежності від форми можуть утворюватися різні види надмолекулярних агрегатів, що згинаються або всередину, або назовні. Відносно міцел ПАР у водному розчині «вигин» шару збудованих поруч одна з одною молекул прийнято називати «спонтанною кривизною» і він знаходиться в прямій залежності від критичного параметра упаковки для індивідуальної молекули.
Поверхнево-активні речовини з великою позитивною спонтанною кривизною (велика голова і маленький хвіст) будуть утворювати агрегати з позитивно (зовнішньо) зігнутим «інтерфейсом». Ясно, що введення таких конусів в ліпідний бішар, який практично не має реальної кривизни, тобто складається з циліндричних молекул, буде викликати напруження. Для модельних систем з чистим ПАР рівень викликаних в мембрані напруг буде залежати не тільки від хімічного складу молекули, але від порядку і рухливості функціональних груп, гідратації, наявних водневих зв’язків, дипольних і електростатичних взаємодій.
Багато «експертів», кажучи про вплив ПАР на ліпідні мембрани, ґрунтуються на припущенні, що всі ПАР працюють в будь-яких умовах однотипно і не враховуються ніякі геометричні ефекти. В такому випадку, дійсно, можна сказати, що вбудовування ПАР в ліпідну мембрану призведе до витончення мембрани і зниження її механічної стабільності а то й до лізису мембрани і витоку вмісту.
А якщо ж так НЕ вважати, то виявиться, що в деяких випадках і при деяких комбінаціях фосфоліпідів і ПАР може відбуватися взагалі зворотний процес - тобто мембрана буде ставати міцніше, а коронавірус - живучішим. У ролі такого прикладу можуть виступати неіоногенні ПАР, які проникаючи в бішари зміцнюють їх. Грішать таким і природні ПАР - сапоніни. Проникнення сапонінів в ліпідну мембрану збільшує її еластичність і пружність щодо деяких синтетичних ПАР.
Таким чином, висновок №3 - ефективність мембрано-руйнівної дії ПАР залежить як від типу ліпідів в мембрані, так і від типу самої поверхнево-активної речовини. Велику роль відіграє фактор кривизни, що утворюються після впровадження ПАР в ліпідний шар агрегатів. При певних умовах ліпідна мембрана не тільки не зруйнується, а навіть стане міцнішою. Ситуація нагадує процес розколювання дров: бувають величезні колоди, які розколоти сокирою важкувато і для цієї мети в деревину заганяють клини. Якщо порівняти форму деяких фосфоліпідів і відповідних ПАР - стає ясно, що клини може знадобиться забивати дуже багато і довго (наприклад, в поєднанні фосфатиділхоліновий ліпид + ПЕГ, або лізолецитиновий ліпид + моноолеін, або фосфатиділетаноламіновий ліпид + лаурилсульфат натрію. Тут потрібно або дуже багато клинів, або використання клина величезного розміру, а значить знову потрібні дослідження.
Крім факторів кривизни, описаних вище, є ще і свої нюанси в типі взаємодій. До сих пір до кінця не встановлено, яка вона є. Наприклад, описана робота, автори якої спробували дуже витончено оцінити механізм взаємодії вірусу грипу і його ліпідної оболонки з різними ПАР використовуючи для цього методи мікрокалориметрії і зміни ентальпії (ΔH) модельної системи вірус - ПАР. Ізотермічна титраційна калориметрия (ITC) використовується для вивчення зв’язуючих властивостей біомолекул і дозволяє безпосередньо виміряти тепло, яке виділяється або поглинається в процесі зв’язування біомолекул. Робиться все це за допомогою мікрокалориметрів:

Негативні і позитивні значення ΔH вказують на екзотермічні і ендотермічні взаємодії відповідно. Екзотермічна взаємодія (з виділенням теплоти) - утворення нових водневих зв’язків (як спирт, який розігрівається при розчиненні в воді) - це електростатична взаємодія. Ендотермічна взаємодія (з поглинанням теплоти) - процес зі збільшенням ентропії - гідрофобна взаємодія - це взаємодія ПАР з ліпідної мембраною.
Система вірус-лауретсульфат натрію (LES) дала позитивну ΔH, що вказує на гідрофобну взаємодію між LES і вірусними частинками, тобто дійсно говорити про вплив на ліпідну мембрану можна. У той же час системи вірус-лаурилсульфат натрію (SDS) і вірус-олеат натрію (C18:1), дали негативні значення ΔH, а значить взаємодії там електростатичні, між молекулами ПАР і вірусними частинками, а ніяк не розчинення мембрани. Притому абсолютне значення ентальпії для олеата натрію було набагато вище, ніж для лаурилсульфата натрію, тобто «оліфа» притягує вірус набагато сильніше. ПАР взаємодіє з мембраною тільки в разі лауретсульфата натрію. Але, серед трьох досліджених поверхнево-активних речовин повсюдно поширений лауретсульфат натрію показав найслабший антивірусний ефект. Автори резонно вважають, що ефективність інактивації вірусу грипу шляхом «розчинення ліпідної мембрани» недостатня навіть щоб запобігти зараженню вірусом грипу. Що ж про коронавірус говорити тоді.
Важливою інформацією є той факт, що має місце бути електростатична взаємодія між негативно зарядженими «головами» SDS і C18:1 і позитивно зарядженими поверхневим білком («шип») вірусу грипу. Гідрофільні групи згаданих ПАР адсорбуються на білку за рахунок електростатики і тим самим інактивують вірус. Але як вже відмічалося вище, для електростатичних взаємодій існує занадто багато обмежень, щоб метод цей можна було впевнено масштабувати для практичного застосування і вивести за рамки «лабораторного досвіду».
У цій же статті автори звертають увагу на те, що при оцінці «противірусної» активності ПАР дуже важливо порівнювати хімічну будову. Наприклад, у SDS гідрофільна група - сульфонова, у C18:1 - карбоксильна. Тобто у SDS великий іонний радіус, у C18:1 - менший. Це говорить про те, що олеат натрію буде набагато слабкіше відштовхуватися від вірусної оболонки ніж SDS, а значить в наявності менше стеричних перешкод і молекула швидше досягне поверхні віріона.
Для розуміння, що таке стеричні перешкоду, подивимось невеличкий колаж з віріонів (без збереження масштабу). Думаю дивлячись на нього зрозуміло, наскільки різними можуть бути поверхні і як важко буде молекулі пробитися до мембрани. Зображення взяті з бази даних вірусних частинок Virus Particle Explorer.
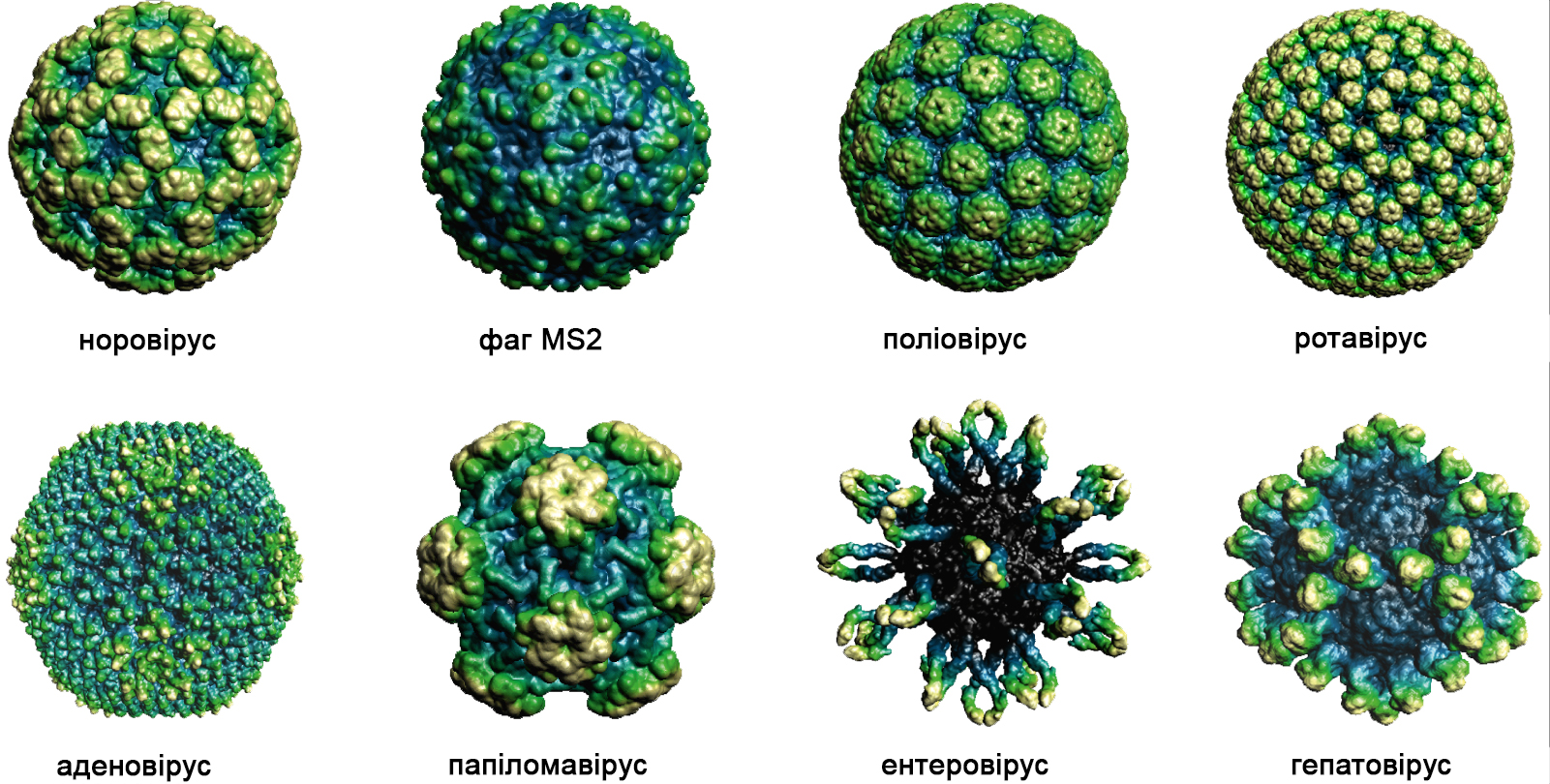
Очевидно, що для ПАР однакового розміру, в однакових умовах, підібратися до ліпідної мембрані і вступити з нею в контакт набагато простіше в разі, наприклад, папіломавірусу, ніж в разі віріона ротавірусу, з його щільно виставленими білковими шипами.
Так що цілком резонно буде відзначити, що електростатичний ефект є кращим в разі інактивації вірусів через мило (на противагу ефекту «руйнування ліпідної мембрани»). Крім того, це надзвичайно швидкий процес (щодо ліпофільних взаємодій, з їх впровадженням ПАР в мембрану, зміною кривизни і т.д.). Але одночасно з цим варто і відзначити те, що досить велику роль в електростатичних взаємодіях займає іонна сила, його pH і навіть валентність іонів, що знаходяться в розчині. Якщо в лабораторних умовах швидше за все використовується деіонізована вода і контролюється рН, то в разі розгляду побутової ситуації всього цього в наявності не буде. Окремо можна причепитися до питання зв’язування ПАР з поверхневими білками. Зв’яжеться воно з будь-якими білками, а не тільки з коронавірусними.
Отже, висновок №4 - В питанні взаємодії ПАР з мікроорганізмом необхідно враховувати тип цієї самої взаємодії. Електростатична вона, чи гідрофільна. Плюс до всього важливим (особливо в разі миття рук) є питання стеричних перешкод «на шляху мила до мембрани». Велика молекула буде добиратися до мішені довше, а то і взагалі не добереться.
5. Нашкірний жир та спиртовий антисептик
До речі, ось жир же - непоганий «антисептик». Та й олія соняшникова поки ще в магазинах є, на відміну від спирту. Так що будь-який із чергових трендів в соцмережах, а там користувачі періодично біжать то за туалетним папером, то за соняшниковою олією, то за гречкою, може виявитися досить недалеко від істини.
Ми вже з’ясували, що по суті, віріон коронавируса - це жирова кулька. Ну а жирова кулька по золотому правилу хімії («подібне розчиняється в подібному») буде змішуватися з ліпофільними речовинами, в т.ч. наприклад з жировими виділеннями шкіри. Чи дасть це якийсь вагомий віруліцидний ефект - сказати складно. Але, наприклад, є стаття, в якій автори згадали про те, що з незрозумілих їм причин природний жировий шар шкіри у деяких людей може надавати бактерицидний ефект на вірус грипу H1N1. Але це у деяких. Всім іншим швидше за все це не загрожує...
Що ж відбувається в процесі миття рук? Наприклад, простою водою. Вода зі своїми водневими зв’язками могла б змити вірус, якби він кріпився тільки водневими зв’язками. Але він «липкий» (як жир) і тримається за рахунок ліпофільних взаємодій (тобто жир розчиняється в жиру). Як спрацює добавка ПАР ми розглядали раніше, тому тепер на дії спирту зупинимося дещо детальніше, благо механізм досить цікавий.
Як вже згадувалося, фосфоліпіди свою надмолекулярну структуру (бішар) утворюють за рахунок слабких взаємодій. А значить, свобода одного закінчується там, де починається свобода іншого, тобто фосфоліпіди можуть рухатися всередині свого шару.
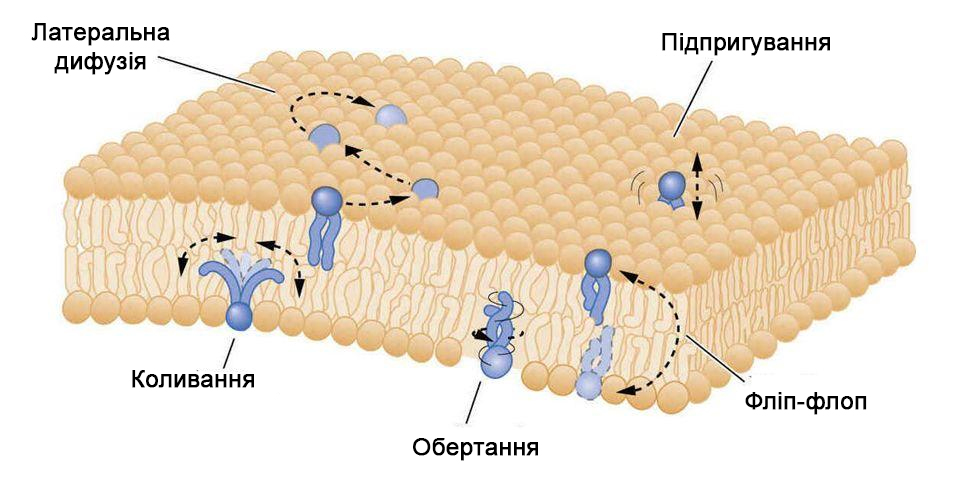
Молекули ліпідів в бішарі знаходяться в постійному русі, якісь обертаються навколо своєї осі, якісь переміщаються, «перекидаючись» з одного боку мембрани на іншу (поперечна, або трансверсальна, або тригерна дифузія), або плавають по одній стороні мембрани (від центру до краю, наприклад). Найрідше має місце поперечна дифузія, тому що перекид вимагає великих витрат енергії, не кожен фосфоліпід може пірнути крізь бішар. Найчастіше має місце поступально-гойдальний рух («тремтіння»). Активність молекул фосфоліпідів в мембрані (наскільки вони неспокійні) визначає таку річ як плинність мембрани, тобто чим вище плинність, тим більш рухливі і схильні до втечі складові частини нашого шару.
Спирт, як вже відмічалося, є більш полярним, ніж вода, а значить з жирами взаємодіє краще, ліпофільніше (неспроста ж їм знежирюють поверхні). Тобто і в мембрани проникає він без проблем, в т.ч., до речі, і в мембрани головного мозку, і гематоенцефалічний бар’єр тут ні до чого чому.
Розглянемо на людському прикладі показати, що з відбувається з ліпідною мембраною під дією спирту:
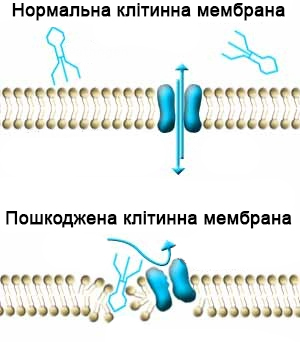
Побачити різницю труднощів не складе. Бачимо діряве решето (зросла проникність мембрани), яке утворюється і в мембрані коронавіруса після контакту зі спиртом (а також, з іншими ліпофільними розчинниками теж, хлороформ або чотирихлористий вуглець будуть діяти ще краще).
Потрапляючи в бішар, етанол за рахунок слабких міжмолекулярних взаємодій прикріплюється до фосфоліпідів і виступає як така собі противага, яка молекулу перекошує.
А де перекіс - там і посилення поступально-гойдального руху, у молекули з’являтися «люфт» (зовсім як у керма в Жигулях). А де люфт, там і кермо може вискочити з рульової колонки. Збільшення рухливості приводить до невпорядкованого стану бішару, збільшення плинності, а значить і проникності. Якщо спирту досить багато - мембрана просто в ньому розпливеться. Головна відмінність спирту від ПАР в його маленькому розмірі. Для нього практично не існують стеричних перешкод, проникає легко і всюди. Тому іноді в біохімії при роботі з вірусами використовуються S/D-підхід (solvent/detergent, тобто розчинник/ПАР). Розчинник підвищує плинність і проникність мембрани абсолютно так само як і ПАР, та й денатурує аналогічно, розкручуючи структуру за рахунок руйнування водневих зв’язків.
Як зрозуміло з усього вищесказаного, є принципова різниця між «інактивацією вірусу» і дезінфекцією. Спирт, як і ПАР, по суті, лише вимикає деякі функціональні елементи вірусу. А та ж перекис водню елементи ці необоротно пошкоджує. Тобто ми як би порівнюємо подію з ймовірністю в 1% і таку ж подію з ймовірністю в 99%.
Досить особисто складно зрозуміти людей, які між мінімальною і максимальною ефективністю чогось вибирають мінімальну, тому що часу або грошей не вистає, покладаючись на те, що авось пронесе і спрацює. Згідно із законом Мерфі «якщо якась неприємність може трапитися, то вона обов’язково трапиться», тому перфекціонізм щодо власної біологічної безпеки ніколи не буде зайвим.
6. Денатурація та ренатурація білків
Після того, як ми розібралися з ліпідними мембранами, прийшов час черконути пару слів і про денатурацію білків (англійська Вікіпедія ставить вказані поняття на один рівень).
Денатурація білків (лат. Denaturatus - позбавлений природних властивостей; від de- - приставка, що означає відділення, видалення + natura - природа, єство) - зміна нативної конформації білкової молекули під дією різних дестабілізуючих факторів. Амінокислотна послідовність білка не змінюється. Призводить до втрати білками їх природних властивостей (розчинності, гідрофільності і ін.). Процес денатурації окремої білкової молекули, що приводить до розпаду її «жорсткої» тривимірної структури, іноді називають плавленням молекули.
Денатурація білків під дією ПАР - це досить складний процес, що протікає в кілька етапів, і по-різному для різних типів поверхнево-активних речовин. Для іонних ПАР (як катіонних, так і аніонних) до якогось рівня концентрацій взагалі не спостерігається будь-яких конформаційних ефектів, тобто немає впливу на розподіл водневих зв’язків всередині білка і будь-яких порушень третинної/четвертинної структури. Потім на початкових стадіях денатурації молекули ПАР за рахунок електростатичних і гідрофобних взаємодій починають чіплятися до амінокислотних залишків. Для аніонних (на кшталт того ж SLS) це катіонні бічні амінокислотні ланцюги (амінокислоти Lys, Arg, His), для катіонних (наприклад, ЧАС) взаємодія йде по аніонних бічним ланцюгах (амінокислоти Glu, Asp). Але і в тому і в тому випадку вуглеводневі "хвости" ПАР будуть зв’язуватися з прилеглими гідрофобними ділянками білка. Знову ж таки, цей механізм застосовується лише для модельної системи (наприклад, білки в біохімічної лабораторії) де відомі концентрації, іонна сила, немає заважають і конкуруючих компонентів і т.п.
Коли всі контактні зони вже заповнені ПАР (при високих концентраціях), накопичення все більшої кількості молекул поверхнево-активної речовини вже може привести до утворення "кластерів", які почнуть розгортати глобулярну структуру білка як клини. Подальше підвищення концентрації ПАР в кінцевому підсумку дозволить кожному білку утворити окремий кластер. Потім залишиться звичайним центрифугуванням розділити білки відповідно до їх молекулярної маси. Швидкість денатурації зростає аж до ККМ, а потім виходить на плато. Тобто в цьому випадку ПАР працює як класичний хімічний денатурант.
Також необхідно сказати і про ренатурацію. Якщо в процесі хімічної обробки зруйновані тільки водневі зв’язки вищих порядків (четвертинна структура, наприклад), і всі зміни пов’язані з переходом з щільно упакованого (упорядкованого) стану в безладний, то є можливість "повернути все назад" за допомогою процесу ренатурації. При нагріванні дволанцюжкових молекул ДНК до температури близько 100 °C водневі зв’язки між основами розриваються, і комплементарні ланцюги розходяться - ДНК денатурує. Однак при повільному охолодженні комплементарні ланцюги можуть знову з’єднуватися в регулярну подвійну спіраль. Ця здатність ДНК до ренатурації використовується для отримання штучних гібридних молекул ДНК (так звана молекулярна гібридизація). Група австралійських і американських хіміків знайшла спосіб (за допомогою використання сечовини і центрифугування) за кілька хвилин ренатурувати куряче яйце, яке варилося 20 хвилин.

З цього слідує, що не варто думати, що мізерними концентраціями ПАР можна незворотньо денатурувати білок вірусу або бактерії, майже як при обробці паром, він може ренатурувати в самий невідповідний момент.
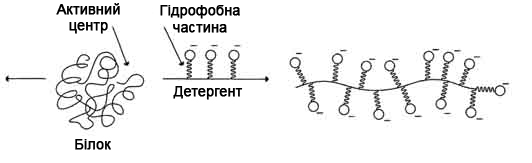
Дослідники за допомогою все тієї ж мікрокалориметрії (ITC) підтвердили те, що молекули ПАР зв’язуються з білками поетапно. При дуже низьких концентраціях (< 0,1 ммоль) ніякого значного впливу не спостерігається. Процес супроводжується підвищеним поглинанням молекул ПАР, а також змінами як у вторинній, так і в третинній структурах білка. З ростом концентрації поверхнево-активної речовини всередині білка поступово починають утворюватися кластери. По досягненню ККМ утворюються міцели (відбувається це в кілька етапів для аніонної ПАР, і відразу - для неіонної ПАР). Тільки в пост-ККМ стані і спостерігається денатурація. Важливим є те, що для неіоногенних і амфотерних ПАР специфічного зв’язування з білком не спостерігається взагалі, аж до концентрацій рівня ККМ. Тобто спостерігається фундаментальна відмінність між денатуруючою здатністю різних класів ПАР, тобто «не всі мило однаково корисно». Можна сказати, що в разі іонних ПАР спостерігається різна динаміка зв’язування для мономерної (нижче ККМ) і міцелярної (вище ККМ) форм існування ПАР в розчині, а для неіонних важливий момент початку процесу міцелоутворення, бо тільки після його початку починає спостерігатися взаємодія зі структурою білка. Якщо говорити простими словами - іонні ПАР можуть взаємодіяти з протеїнами в будь-якій формі, неіоногенні і амфотерні - тільки в формі міцел, а до утворення міцел їх ще потрібно відповідним чином довести.
Отже якщо все ж таки вирішено замінити всі деззасоби на мило, то для початку треба дізнатися, який склад має мило та підрахувати, скільки годин потрібно милити для ККМ.
До речі, денатуруюча здатність ПАР по відношенню до білків - це, в деякому роді, взаємовиключна позиція по відношенню до ліпідів. Взаємовиключна тому, що «ПАР витрачаються на білки, а для ліпідів їх вже не вистачає», отже, доведеться вибирати щось одне. Деяким підтвердженням сказаного вище може бути і стаття, в якій розглянуто механізм дії ПАР Triton X-100 на вірус грипу. У роботі використовувався 1% розчин (17 ммоль), в якому концентрація ПАР значно вище критичної концентрації міцел (від 0,2 до 0,9 ммоль). У статті автори вказують, що оскільки критична концентрація міцел Triton X-100 залежить від температури, а повна солюбілізація цього ПАР при даній концентрації залежить від кількості мембран і білка в розчині, то слід адаптувати умови під конкретний метод і конкретну систему (температура - параметри водного середовища - тривалість обробки). Використання систем з більш високим вмістом білка або ліпідів негативно впливає на інактивацію і вимагає постійного збільшення концентрації ПАР.
Для більшої об’єктивності все ж варто відзначити, що крім впливу на нековалентні взаємодії, ПАР іноді можуть каталізувати і утворення нових ковалентних («сильних» зв’язків). Як приклад цієї нехарактерної особливості можна, наприклад, згадати кислотний гідроліз амідних і пептидних зв’язків (при pH нижче 3,0 і температурі > 37 °C). Тобто ніяких там надмолекулярних структур, все просто. Сильнокисле середовище, температура «гарячкового стану»... Цілком повсякденні умови.
Окремо хотілося б сказати про денатурацію білків спиртом. Взагалі не зрозуміло, деякі автори пишуть, що мило денатурує білки краще спирту. Хоча принципово механізм однаковий - все той же розрив водневих зв’язків і «розклинення» структури білка.
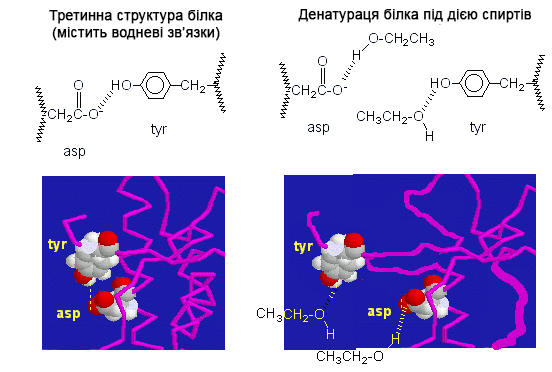
На малюнку ми бачимо, що водневий зв’язок утворюється між різними амінокислотами. У разі контакту зі спиртом (схожим чином, до речі, буде діяти і ацетон, і діетиловий ефір і ще багато чого, але спирт самий біогенний) міжмолекулярні водневі зв’язки руйнуються. Амінокислоти зв’язуються вже з молекулами спирту, а не один з одним. І так лавиноподібно білок втрачає свою структуру, а з нею і функціонал, тобто денатурує.
Отже висновок №5 - «мило денатурує білки» тільки в лабораторних умовах. Тут ситуація повністю повторює написане для висновку №2. Величезні концентрації, чисті водорозчинні (НЕ поверхневі) білки... І бонусом можливість ренатурації. Порівнювати денатуруючу здатність по відношенню до білків між спиртом і милом - верх самовпевненості (і недалекоглядності тих, хто це радить робити).
7. Шкідливий вплив мила
Як казав Парацельс: «Все - отрута, все - ліки; те й інше визначає доза».
Було б нерозумно вважати, що раз мило і ПАР потенційно здатні «створювати діри» в клітинних мембранах, то мембрани самої людини така доля не спіткає. Спіткає, та ще й як. Чому? А тому що всередині нашого організму теж ліпідний бішар. І бішар цей складається з абсолютно таких же фосфоліпідів, як і у бактерії кишкової палички або коронавіруса (ну не абсолютно таких же, невеликі хімічні відмінності є, але вони не критичні в застосуванні до світу тонких взаємодій).
Найчастіше від ПАР страждає шкіра, так як саме шкіра першою контактує з різними миючими засобами. Можна і зубну пасту з SLS згадати, слизова оболонка рота впустить поверхнево-активні речовини в свої мембрани набагато швидше ніж груба ороговіла шкіра. До речі, щодо шкіри, ефект подразнення/руйнування посилюється в ряду неіоногенні ПАВ → амфотерні ПАВ → аніонні ПАВ → катіонні ПАР. Тобто найбільш сильними є ЧАС.
Було проведене дослідження, в якому автори визначили інгібуючі концентрації декількох технічно значущих поверхнево-активних речовин для кератиноцитів.
Кератиноцити - основні клітини епідермісу шкіри людини (складають приблизно 90% всіх клітин епідермісу).
Перевіряли лаурилсульфат натрію (SLS), лауретсульфат натрію (SLES), кокоамфоацетат натрію (SCAA), кокамідопропілбетаїн (CAPB) і лаурілглікозід/кокоглікозід, тобто все те, що зустрічається в 99% косметичних засобів і засобів по догляду за шкірою. В результаті виявилося, що застосування ПАВ змінює рівні експресії для ферментів, які беруть участь в біосинтезі мембранних компонентів, таких як холестерин, кераміди і жирні кислоти. Використовуючи ПАР ми позбавляємо свою шкіру важливих бар’єрних функцій. Також в статті досліджували конкретно вплив ПАР на жири рогового шару.
Взагалі у людей аніонні ПАР найчастіше призводять до дерматитів, або афтозних виразок, по типу афти чи стоматиту і т.п. Через високу молекулярну масу і, відповідно, слабку адсорбцію в кишечнику, отримати гостре токсичне отруєння ніби як важко, але цілком реальна поява деяких хронічних ефектів за рахунок отримання і накопичення ПАР з питної води, миючих засобів, зубної пасти і їжі.
Висновок №6 - Було б дивно вважати, що те, що розчиняє ліпідні мембрани в мікроорганізмі не буде їх розчиняти або робити більш проникними в організмі-носії (тобто у людини). Страждати буде в першу чергу шкіра. По-друге - шлунково-кишковий тракт, так як змивати ПАР потрібно ще вміти, і вони все одно потрапляють разом з їжею. Гаразд би для мембран кишечника це буде «укус комара» (якщо не пити fairy), а ось для мембран мікробіоти - навіть невелика кількість ПАР може стати фатальною. А мікробіота - це наш імунітет.
8. Шляхи поширення коронавірусу
На сьогоднішній день вважається, що важливий нам коронавірус поширюється при безпосередньому контакті, на фомітах, а також за допомогою повітряно-краплинного шляху (через біоаерозлі, які утворюються при кашлі, чханні і розмові).
Фоміти (англ. Fomites) - будь-які предмети, контаміновані патогенними мікроорганізмами або іншими паразитами, при зіткненні з якими виникає ризик зараження. Типовими фомітами є одяг, поверхня шкіри, волосся, а також постільні приналежності в медичних установах.
Найчастіше типовий громадянин боїться того, що хтось чхне або буде кашляти і аерозоль з віріонами полетить і осяде на ньому самому. Але не менш важливий для зараження і тактильний контакт.
Виживання мікроорганізмів на фомітах (та й на руках теж) визначають декілька факторів:
1. Характеристики фоміта (особливості поверхні, пористість і т. п.).
2. Зовнішні чинники (температура і вологість середовища).
3. Характер і частота контактів з фомітом.
Тут найцікавіший і самий слабо вивчений в плані механізмів пункт - це «поверхневі характеристики фоміта».
Отже обсіменіння поверхонь (фомітів) може відбуватися в тому числі і завдяки осіданню біоаерозолів. Адже якщо подивитися більш прецизійно, то виявиться, що слина (або інша біологічна слиз) складається з різних електролітів (натрію, калію, кальцію, магнію, бікарбонат- і фосфат-іонів) + імуноглобуліни, білки, ферменти, муцини і азотисті продукти (сечовина і аміак). Тобто при чханні вилітають не тільки віріони, а й купа органічних сполук, в основному білкової природи. Найбільш цікавим об’єктом є саме муцини. Вони до того ж є основним компонентом, що входять до складу секрету всіх слизових залоз.
Високомолекулярний муцин, який адсорбується на поверхні, служить для змащування поверхонь, труться між собою (наприклад, ротова порожнина і їжа), а вільний муцин, що знаходиться в обсязі секрету слинних залоз, є колоїдним стабілізатором і регулює в’язкість і пружність слини. Тому будь-яка їжа і напої можуть взаємодіяти з білками слини як на поверхні, так і в об’ємі розчину (за рахунок фізико-хімічних взаємодій або зміни конформації білків слини) і активно впливати на склад і реологічні властивості слини.
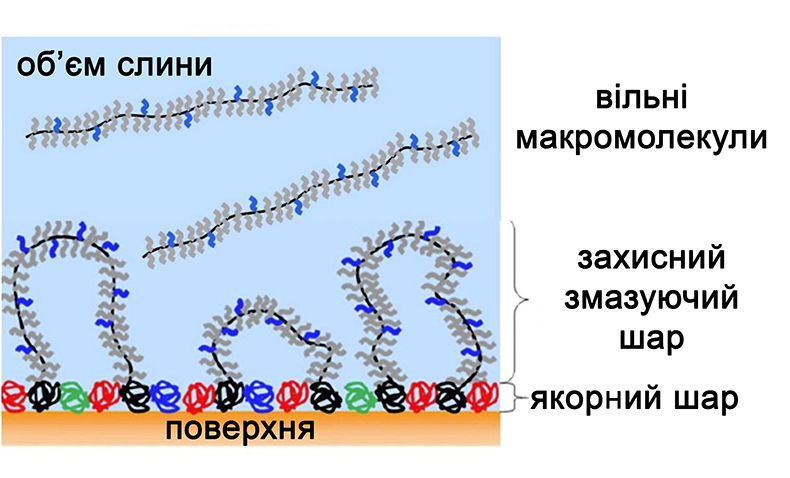
Молекула муцина, а в слині присутні муцин-1 (молекулярна маса 250 кДа) і муцин-2 (молекулярна маса 100 кДа), схожа на гребінку і складається з білкової частини (суцільна лінія з пептидів) і коротких полісахаридних ланцюжків, що складаються з фруктози, галактози, N-ацетилглюкозамін та інших цукрів. Маючи гелеобразную консистенцію, ці глікопротеїни зв’язують велику кількість води і забезпечують рівномірну змазку (за рахунок зниження коефіцієнта тертя) і зволоження порожнини рота. Муцини утворюють бар’єр і захищають чутливі слизові оболонки від висихання і хімічних і механічних впливів.
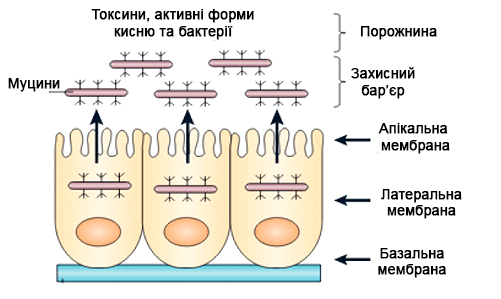
У нормальному стані поверхня язика і ротової порожнини покрита рівномірною тонкою плівкою слини, що містить муцини. При контакті з продуктами, що містять в’яжучі (дубильні речовини) компоненти, муцини, як і будь-які інші білки вступають в хімічну взаємодію з танінами. Знижується їх розчинність в воді, відбувається агрегація і навіть випадання в осад. Тобто після контакту з таніном, гладка глянцева поверхня, змащена муцин-вмісною слиною починає нагадувати шорсткий наждачний папір, сформований безліччю мікро-дір. Тобто в найпростішому застосуванні, терпкий смак - це коли язик стає менш слизьким.
Білки при висиханні і денатурації формуватимуть досить стійкі білкові біоплівки. А біоплівку вже просто милом не взяти. Потрібна «проста жорстка хімія», на кшталт перекису або гіпохлориту натрію. А крім того, саме на денатурацію білкового носія з мокротиння та соплі, а не мембранного білка коронавіруса, буде в першу чергу витрачатися та сама найдорожча поверхнево-активна речовина.
Підсумуємо, в навколишньому середовищі мікроорганізми не подорожують без нічого (у вигляді індивідуальних віріонів). І не дивлячись на те, що в пробірці, в лабораторних умовах, добавка розчину ПАР змушує мікроорганізми гинути, в умовах реального життя (контамінація рук забрудненнями різної хімічної природи з віріонами коронавіруса в ролі пасажирів) це абсолютно ідеалістичний, а то і небезпечний підхід.
Таким чином, підсумок №7 - Слід враховувати, що при висиханні крапельних біологічних аерозолів («напівфабрикат» кашлю та чхання) можуть утворюватися досить стабільні білкові плівки, проникнути в які і знищити віріон, що там знаходиться, зможе тільки жорсткий дезінфектант на кшалт перекису водню і т.п.
9. Коли гідродинаміка важливіше за ПАР
Гідродинаміка (від грец. Ὕδωρ «вода» + динаміка) - розділ фізики суцільних середовищ, що вивчає рух ідеальних і реальних рідин і газу та їх силову взаємодія з твердими тілами.
У загальному і цілому гідродинаміка важлива для будь-якої ситуації, де рідина стикається з твердими тілами, процеси миття та дезінфекції не виняток. Завжди варто тримати в умі наявність шорсткостей, нерівностей і т.п. (особливо в разі пористих поверхонь).
На жаль, сказати що ця область вивчена фрагментарно - не сказати нічого. Лічені дослідники (найчастіше хіміки поверхонь) починають замислюватися (тільки замислюватися) про вплив мікроструктури поверхні на ефективність роботи рідких контактних дезінфікуючих засобів і т.п. А те, що вплив цей є - безумовний факт. Непрямим підтвердженням цього є, наприклад, робота, в якій дослідники виявили, що гідродинамічні параметри (швидкість потоку, режими перемішування і т.д.) потоку води, якою миють овочі, чинить серйозний вплив на кількість живуть на поверхні популяцій кишкової палички. В результаті прийшли до того, що необхідно або використання дезінфікуючого засобу (типу перекису, або білизни), або ж оптимізувати швидкість потоку, його режим (турбулентний/ламінарний) та час обробки.
Очікувати подібних досліджень, але присвячених гідродинаміки процесів миття рук - навіть і мріяти не варто, принаймні найближчим часом. Але слід зауважити, що «рекомендацій від лікарів» де вони вивчають ефективність «активного миття рук» (хоча б за методикою ВООЗ) - вистачає.
Останній висновок №8 - Незважаючи на практично повну відсутність досліджень впливу гідродинаміки при митті рук, враховувати цей фактор варто. Тобто не просто щось там замочувати в розчині, а замочувати активно, змінюючи режими роботи потоку, його швидкість і час обробки. Адже навіть шкіра шорстка і зморшкувата на мікрорівні і потрібна неабияка кількість втирання і «просочення», щоб ті ж ПАР проникли в кожні поглиблення, де потенційно може поміститися віріон 100 нм діаметром. Чого вже говорити про якісь пластики або тканини...
Висновки
Ну а тепер зберемо наші висновки воєдино, для підсумування пройденого матеріалу.
Чи достатньо миття рук для захисту від коронавируса? Ні, недостатньо тому що:
1. В теорії руйнування ліпідної мембрани можливо за рахунок утворення міцел, що забирають в собі (солюбілізують) структурні елементи вірусної оболонки (фосфоліпіди). Міцели завжди утворюються при концентраціях близьких до ККМ. Концентрації ці абсолютно різні для різних ПАР і залежать від температури, від хімічної природи поверхнево-активної речовини, від іонної сили розчину і т.д. і т.п. Привести до спільного знаменника всі ці фактори навіть для одного чистого ПАР - робота не одного місяця для цілого НДІ. Публікацій з описом таких взаємозв’язків - не виявлено
2. Крім ефекту солюбілізації може мати місце ефект порушення цілісності ліпідної мембрани (утворення пір), які при lim → ∞ дадуть порушення цілісності оболонки і ліквідацію віріона. Ефективність цього процесу також залежить від концентрації ПАР, динаміки вбудовування в мембрану і критичного параметра упаковки ПАР. Так як ці фактори в разі НЕ лабораторних випробувань носять абсолютно випадковий характер, то результат буде теж абсолютно випадковим. А значить, його можна не враховувати. Публікацій з оцінкою вірогідності такого процесу - не виявлено. При обліку параметра упаковки може так статися, що ПАР з невідповідною структурою замість руйнування вірусної мембрани зміцнять її (змінять спонтанну кривизну не так як хотілося б). Такий ефект може мати місце для неіоногенних ПАР і деяких природних ПАР (на кшталт сапонінів). Так що не всі «еко-біо-мила» однаково корисні, і це ще м’яко кажучи.
3. Крім гідрофільних взаємодій (розчиняти мембрану) ПАР можуть взаємодіяти з колючкуватими білками вірусу за рахунок електростатичної взаємодії. Притому різні ПАР будуть абсолютно по-різному проявляти себе, це буде залежати як від хімічної природи мила (розміри і форма «голови» і «хвоста»), так і від доступності колючкуватих білків віріона для взаємодії (стеричні перешкоди). Питання це вивчено дуже фрагментарно для вірусів в цілому, і не вивчено взагалі для коронавіруса зокрема. Всі доводи можуть бути виведені тільки на підставі екстраполяції.
4. У теорії інактивація вірусу можлива за рахунок денатурації (руйнування третинної або четвертинної структури) колючкуватих білків вірусу. Але як і в першому випадку тут грає роль і концентрація ПАР, і рН і іонна сила і наявність речовин, що заважають реакції (не колючкуваті білки, а наприклад, білки біоплівок або забруднень). Крім того, ефективність денатурації безпосередньо залежить від типу ПАР. Іоногенні речовини мають ефективність зростаючу з концентрацією ПАР в розчині, неіоногенні - починають порушувати структуру білка тільки при досягненні ККМ. І найголовніше, все міркування побудовані на припущенні про те, що денатурація відбувається певним чином на прикладі статей де вивчали розчинні у воді білки. Статей з описом оцінки ефективності практичної денатурації поверхневих мембранних білків вірусів за допомогою ПАР - не виявлено. А масштабувати явища макросвіту на мікросвіт - справа невдячна.
5. Не можна вважати панацеєю і спирт, який як і ПАР, по суті, лише вимикає деякі функціональні елементи віріонів. Робити він це може двома різними шляхами - проникненням в ліпідну мембрану і створенням пір (так само, як описано для ПАР), так і денатуруючи білки. В цьому плані спирт нічим не відрізняється від ПАР, з тією лише різницею, що завдяки малому розміру проникає швидше (але і випаровується швидше). Можна припустити, що якщо порівняти всі фактори - один одного вони будуть коштувати. Так що ні спирт, ні ЧАС не дають при невеликих експозиціях (мають місце при обробці рук) 100% ймовірності повного знезараження через особливості своєї дії і впливу на цю дію умов обробки (геометрія поверхні, наявність речовин-антагоністів і т.п. ). Не варто випробовувати долю і грати з коронавірусом (а ще кишковою паличкою, паліовірусом, стафіллококком і т.п.) в російську рулетку. Також, в теорії, схожим «знезаражувальним» ефектом будуть володіти і багато інших розчинники, які здатні змішуватися з жирами («знежирювачі»), хлороформ наприклад.
Що ж залишається? Та все ті ж, старі друзі - перекис і гіпохлорит. Оптимальним буде наступний алгоритм обробки: мити руки з милом НЕ 20 секунд, як радять деякі «лікарі», а стільки секунд, скільки потрібно щоб виконати інструкцію ВООЗ з миття (при параної виконати можна кілька разів). Принцип як у відомій фразі про те, що «працювати треба не з 8 до 17, а головою». Чисті, підготовлені руки - обробляємо засобами, що містять активні дезінфектанти - перекис водню (від 0,5%), гіпохлорит натрію (від 0,01-0,05%) або розчином хлорціануратів порівнянних з гіпохлоритом концентрацій. І обробляти найкраще зануренням в ємність з розчином, а не розмазування по руках. І ось тут без мила вже погано бо: забруднення на руках і немає миття - антисептик не спрацює або спрацює погано, а миття тільки милом - вірогідність не змити взагалі або змити далеко не всі. І, в будь-якому випадку, перед тим як щось робити, потрібно хоча б на свої руки подивитися уважно.
Література
Бесараб С.В. Избранные главы коллоидной химии. Достаточно ли мытья рук для защиты от коронавируса? «Мыльная энциклопедия» [Электронный ресурс] – Режим доступа: https://habr.com/ru/post/503482













